
In situ-generated vaccine-like pyroptosome for personalized cancer immunotherapy
原位生成的类疫苗焦亡小体用于个性化癌症免疫疗法
论文信息:Binlong Chen 1,2,9 , Fangjie Wan2,9, Heming Xia2, Xingquan Pan2, Letong Wang2, Yaoqi Wang3, Yue Yan4, Jianxiong Liu2, Mingmei Tang2, Ye Yang2, Mengmeng Qin 2, Jiaona Ren2, Bushu Zhou2, Lijun Zhong5, Wei Chen1, Chuanhui Han6,7, Mi Deng 6,7, Qiang Zhang 1,2 & Yiguang Wang 1,2,8https://doi.org/10.1038/s41563-026-02506-9
主讲人:邝宣诚,2024年4月19日
研究进展 or 研究背景:
大多数肿瘤中癌症-免疫周期多个关键步骤的时空协调性差以及与治疗策略相关的全身毒性,阻碍了原位癌症疫苗接种的功效。
我们在此报道了一种可全身注射且可诱导焦亡的纳米佐剂,该佐剂可在肿瘤区域诱导疫苗样焦亡小体的分泌,从而产生强大的抗肿瘤免疫。
这种可全身注射且可诱导焦亡的纳米佐剂可诱导剧烈的免疫原性焦亡,触发富含肿瘤抗原的焦亡小体、损伤相关分子模式和促炎细胞因子的有效释放。
将TLR7/8激动剂光激活释放至焦亡小体中,构建了一个原位癌症疫苗平台,该平台可协同激活癌症-免疫周期并避免全身毒性。
该疫苗可同时增强先天性和适应性免疫反应,促进原发肿瘤和转移结节的清除,从而提供持久的癌症预防。总而言之,此处报道的用于增强癌症-免疫周期的诱导焦亡纳米药物的合理设计,可能有助于开发更有效的个性化癌症免疫治疗方法。
解决方案 or 研究内容:
原位癌疫苗接种需要协调激活癌症-免疫周期(CIC),包括死亡癌细胞的抗原释放、抗原呈递细胞(APC)的抗原处理和呈递,以及肿瘤特异性效应T细胞的生成以裂解肿瘤细胞,从而进一步增强CIC7,8。然而,CIC中每一步的限速能力以及免疫抑制性肿瘤微环境对CIC的高效激活和随后的抗肿瘤免疫反应构成了重大挑战9。已开发出多种策略来放大CIC,包括与细菌膜杂交10、与氟聚合物协同作用11、与免疫佐剂联合12、与mRNA疗法整合13以及广泛研究的化学/放射疗法介导的免疫原性细胞死亡(ICD)14。光疗,特别是光动力疗法(PDT),通过在光照下选择性激活光敏剂负载的肿瘤细胞,提供高度局部化的治疗,从而最大限度地减少脱靶效应,并相对于其他治疗策略具有显著优势。越来越多的证据表明,死亡的性质决定了CIC的启动15,16。最近,凋亡被认为是一种很大程度上免疫沉默的细胞死亡形式,其特征是自我降解和细胞内容物释放极少17。相比之下,程序性坏死(programmed necrosis)的裂解性质优化了抗原和佐剂的提供,从而增强了CIC,产生了强效的肿瘤特异性T细胞免疫。因此,迫切需要利用程序性坏死细胞死亡,通过高效的CIC级联放大来实现原位癌疫苗接种。
要点:
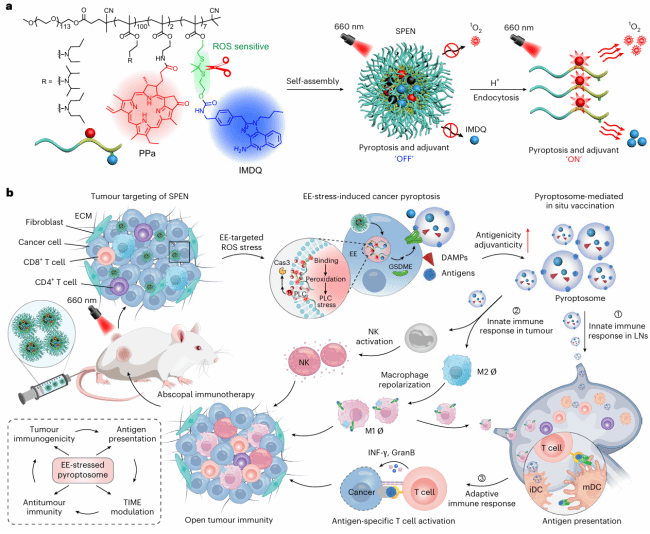
通过原位光引发类疫苗焦亡小体增强细胞免疫清除(CIC)的空间光控免疫纳米平台(SPEN)示意图。a,pH 与光控纳米佐剂的设计思路:该佐剂通过靶向早期内体的应激反应,诱导癌细胞发生特异性免疫原性焦亡,实现原位肿瘤疫苗化。b,SPEN 在血液循环及胞外分布阶段,其焦亡诱导活性与佐剂活性均处于 “关闭” 状态;在肿瘤富集并被细胞内吞后,SPEN 通过早期内体定位的氧化应激(SPEN<sub>EE</sub>)特异性触发癌细胞焦亡,并释放 Toll 样受体激动剂 IMDQ,同步激活细胞免疫清除效应与佐剂活性。凭借高效的焦亡诱导能力,SPEN<sub>EE</sub>技术可根除原发肿瘤,随后形成包含肿瘤抗原与 IMDQ 的类疫苗焦亡小体。该焦亡小体通过特异性增强肿瘤组织中巨噬细胞与树突状细胞的抗原呈递作用,发挥原位疫苗功能,重塑肿瘤及淋巴结的免疫微环境,从而实现强效且持久的肿瘤免疫治疗。TIME,肿瘤免疫微环境;GranB,颗粒酶 B;iDC,未成熟树突状细胞;mDC,成熟树突状细胞。
总结与展望:
特异性肿瘤抗原的免疫原性弱且可用性差,是阻碍癌症疫苗临床治疗效果的主要障碍3,29。原位癌症疫苗利用肿瘤部位的自体肿瘤抗原,已被提议作为术后个性化癌症免疫疗法11。为了优化原位肿瘤疫苗的免疫原性,人们采用了各种策略,包括化疗30、放疗31、光疗32和溶瘤病毒疗法33,将其用作细胞应激诱导剂以触发免疫原性细胞死亡(ICD)。然而,癌症免疫与细胞器应激诱导的ICD效应之间的免疫学相关性,以及其潜在的免疫原性机制仍不清楚。得益于我们具有时空可调性的焦亡纳米技术,我们成功地在体外和体内揭示了癌细胞免疫原性依赖于细胞器应激的扩增机制。我们进一步开发了一种SPEN,通过增强癌症免疫循环(CIC)来充当原位癌症疫苗。这项研究不仅证明了受能量应激(EE)影响的焦亡细胞死亡的显著免疫原性功能,揭示了焦亡来源囊泡的潜在免疫启动机制,还为设计用于个性化癌症免疫疗法的焦亡诱导纳米材料开辟了新的机会。

