引言:
从机械力感知到细胞决策——力学信号转导开启伤口愈合新视野
皮肤作为人体最大的器官,其完整性对维持机体内环境稳定至关重要。当组织受损时,机体通常会启动一系列精密调控的生物学反应以促进修复。然而,糖尿病、衰老、长期卧床等病理状态会严重阻碍这一过程,导致伤口停滞在炎症阶段,演变为慢性难愈合溃疡。
传统临床治疗方法虽然能提供一定缓解,但效果往往不尽如人意。清创和敷料治疗周期长、抗生素面临耐药性问题、负压伤口治疗虽有效但成本高昂且操作复杂。因此,研究重点正从单纯关注生物化学信号转向探索生物物理与生物化学通路的交叉融合。
近日,山西医科大学第一医院的研究团队在《iScience》发表综述,系统阐述了Piezo1-PI3K/Akt信号轴作为皮肤伤口愈合中上下文依赖型力学转导节点的分子机制与功能意义,为开发基于力学调控的创新伤口治疗策略提供了全新思路。
一、力学信号在皮肤伤口愈合中的关键作用
机械力已被证明通过力学转导通路影响皮肤组织再生。现有证据表明,机械力可精细调控成纤维细胞、角质形成细胞和血管内皮细胞的活性,进而促进细胞外基质重塑和组织愈合。
机械应力的精细管理对维持基质沉积平衡、促进成纤维细胞向肌成纤维细胞转化、以及预防病理性纤维化和增生性瘢痕形成至关重要。
【图1|Piezo1通道的结构架构与力学门控机制】
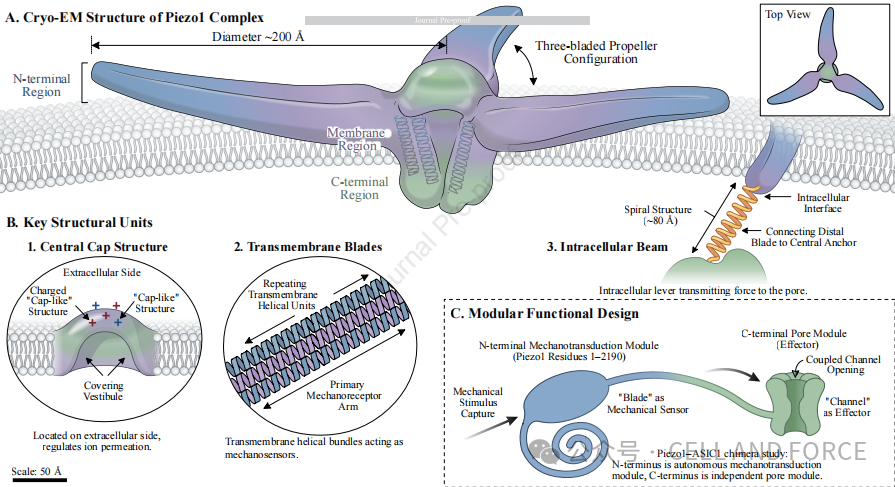
图1A展示了Piezo1复合物的同源三聚体结构,呈三叶螺旋桨构型,直径约200Å。这种独特的结构通过冷冻电镜得以解析,揭示了中央帽状结构、跨膜结构域和整体分子构架。
图1B标示了三个关键结构单元:
图1C展示了基于Piezo1-ASIC1嵌合体研究的功能域组织:
二、Piezo1:从力学感知到生化信号的转换器
2.1 Piezo1的发现与结构特征
2010年,研究者发现了Piezo蛋白家族(Piezo1和Piezo2),这是一类全新的机械激活阳离子通道。与传统电压门控或配体门控通道不同,Piezo1具有独特的同源三聚体结构。
当被激活时,Piezo1允许阳离子(主要是Ca²⁺,以及Na⁺、K⁺、Mg²⁺)进入细胞。作为经典的第二信使,Ca²⁺通过改变其在时间和空间上的浓度,启动多种信号通路,包括钙调磷酸酶/NFAT、YAP/TAZ和PI3K/Akt。
2.2 Piezo1的离子选择性与Ca²⁺通透性
尽管Piezo1也允许Na⁺和K⁺通过,但其主要功能是优先选择Ca²⁺——这一特性在心肌细胞、血管内皮细胞和免疫细胞中均被观察到。这种离子选择性归因于通道独特的三维构象:张力诱导的孔道构象变化与特定氨基酸残基相互作用,动态调节对Ca²⁺的亲和力和通透性。
2.3 Piezo1作为“精准时空信号编码器”
Piezo1介导的Ca²⁺信号不是简单的细胞内钙水平持续升高,而是呈现复杂的时空动态。
时间维度:在HEK293T细胞和小鼠胚胎血管内皮细胞中,层流剪切应力可直接刺激Piezo1,产生快速适应的内向电流——通道开放后迅速失活,产生短暂的电流信号而非持续去极化。在人神经干细胞中,牵引力激活的Piezo1诱导秒级自发Ca²⁺瞬变。这种具有特定频率和波形的Ca²⁺振荡代表了一种“频率编码”系统,使细胞能够区分不同类型和强度的机械刺激。
空间维度:在血管内皮细胞中,剪切应力促使Piezo1向顶面片状伪足前缘移动和聚集,对细胞极化和定向排列至关重要。这表明Ca²⁺内流并非均匀分布在细胞各处,而是局限于特定亚细胞区域,形成局部Ca²⁺微结构域。
三、从离子流到激酶级联:四种分子桥梁
Piezo1介导的Ca²⁺内流如何激活PI3K/Akt信号通路?研究团队系统梳理了四条并行的分子桥梁,并在成纤维细胞中评估了每条通路的验证程度。
【图2|Piezo1介导Ca²⁺内流与PI3K/Akt激活的四种分子桥梁】
3.1 直接通路:CaM/CaMK介导的激活
CaM-pY99通路:当Ca²⁺结合钙调蛋白(CaM)时,触发Tyr99位点的显著磷酸化修饰,产生高亲和力的pY99-CaM。这种磷酸化形式的CaM可结合Class I PI3Kα调节亚基p85的SH2结构域,解除p85对p110催化亚基的自身抑制,激活PI3K/Akt。
验证状态:该通路的生化机制在实验室重构研究和癌细胞模型中已充分证实,但在真皮成纤维细胞中尚未直接验证。上游酪氨酸激酶(Src家族激酶)仅在KRAS突变癌细胞中明确,机械刺激成纤维细胞中的激酶身份尚不明确。
CaMKK-Akt直接通路:Ca²⁺/CaM复合物激活CaMKK,进而直接刺激Akt——这一过程可不依赖PI3K。
3.2 协同通路:Integrin-FAK-PI3K/Akt
这是目前在真皮成纤维细胞中验证最充分的通路。
整合素-黏着斑:整合素作为物理锚点感知基质刚度并促进细胞骨架张力发展,而Piezo1作为张力的次级感受器。Yao等(2022)发现,随着人包皮成纤维细胞铺展,Piezo1在30-60分钟内逐渐聚集于应力纤维末端的成熟黏着斑。FRAP研究显示,Piezo1在黏着斑的停留时间(t₁/₂≈120秒)显著长于Paxillin(≈25秒)和整合素β3(≈90秒)。
Chen等(2023)证明,Piezo1依赖的Ca²⁺内流可显著增强FAK Y397位点的磷酸化水平。磷酸化的FAK通过SH2结构域相互作用招募PI3K的p85调节亚基,激活下游信号。
验证状态:该通路在三个维度(机制验证、细胞类型特异性、伤口愈合功能相关性)均获得最强证据支持。唯一的缺口是:完整信号链尚未在单个成纤维细胞实验中作为连续、实时序列得到验证。
3.3 CADM1:延长Piezo1激活的关键分子
Koster等(2024)利用邻近标记技术绘制Piezo1表面相互作用组,发现CADM1(细胞粘附分子1)通过与Piezo1跨膜结构域相互作用,显著延长Piezo1的开放状态并延迟其失活。这为Piezo1维持长时间Ca²⁺信号、进而激活FAK和PI3K/Akt通路提供了新机制。
3.4 调节机制:Calpain的双重作用
Calpain是一类Ca²⁺依赖的半胱氨酸蛋白酶,对PI3K/Akt信号通路呈现上下文依赖的双重调节:
验证状态:该机制在成纤维细胞中尚未直接验证,双相调节模型是从乳腺癌和听觉系统研究外推而来,应视为推测性的。
3.5 旁分泌机制:ATP-P2Y2通路
Piezo1激活后的ATP释放并非直接通过离子通道,而是依赖下游Ca²⁺效应器:
验证状态:Piezo1→PANX1→ATP释放机制主要在红细胞、内皮细胞和胆管细胞中证实。虽然在成纤维细胞中PANX1广泛表达、P2Y2表达已确认,但Piezo1触发PANX1依赖性ATP释放尚未在真皮成纤维细胞中直接证明。
四、PI3K/Akt信号轴对成纤维细胞命运的精细调控
【图3|PI3K/Akt信号枢纽调控成纤维细胞的四大功能】
4.1 细胞增殖
Zhang等(2024)在瘢痕疙瘩组织中发现了一类对机械拉伸特别敏感的CD74⁺成纤维细胞亚群。机械力激活这些细胞膜上的Piezo1通道,导致钙离子内流和Akt磷酸化显著增加。使用siRNA沉默Piezo1可有效抑制拉伸诱导的Akt磷酸化和成纤维细胞增殖。
在分子层面,激活的Akt磷酸化并抑制GSK3β,阻止其对Cyclin D1的降解,导致Cyclin D1稳定积累和核转位,直接促进细胞周期进程。PI3K抑制剂LY294002可完全抑制Piezo1激动剂Yoda1诱导的抗凋亡和促增殖作用。
4.2 细胞骨架重塑与迁移
Piezo1/FAK/Akt轴的存在已在胶质母细胞瘤模型中得到验证。在真皮成纤维细胞中:
Piezo1响应机械力与成熟黏着斑结合(Yao 2022)
Piezo1介导的Ca²⁺内流显著增强FAK Y397磷酸化(Chen 2023)
FAK磷酸化通过招募PI3K p85亚基激活PI3K/Akt(Xia 2004)
空间定位机制:Piezo1在迁移细胞的前沿富集于片状伪足和丝状伪足尖端,在此区域感知膜张力并促进局部Ca²⁺微结构域形成,进而促进肌动蛋白聚合和细胞骨架快速重塑。Yang等(2022)发现,Piezo1三聚体的大穹顶状结构优先定位于平坦或凹陷膜区域,而天然排除于高曲率区域(如外向突起),这一物理特性有助于防止Piezo1在伪足尖端的随机激活,维持细胞定向迁移。
细胞类型特异性:Piezo1对细胞运动的影响具有高度细胞类型特异性。在角质形成细胞中,Piezo1聚集于细胞后部,通过促进局部回缩来减慢迁移;而在成纤维细胞中,Piezo1-PI3K/Akt通路通常促进迁移和侵袭。
4.3 成纤维细胞活化与基质合成
TGF-β/Smad通路与机械力的协同作用:TGF-β通过SMAD依赖和替代途径促进成纤维细胞活化、EMT、ECM积累和肌成纤维细胞转化。Xu等(2025)在肺纤维化模型中首次在体内证明了Piezo1与TGF-β/Smad之间的直接调控联系——在Periostin⁺肌成纤维细胞中靶向敲除Piezo1显著降低了促纤维化基因表达。
PI3K/Akt与Smad信号通路之间存在复杂的交互作用:
ECM合成的分子调控:Byun等(2024)在皮肤再生模型中揭示了“Piezo1-Akt-mTOR”合成通路。PLLA微球的机械刺激激活成纤维细胞膜上的Piezo1通道,导致Ca²⁺内流和Akt磷酸化,激活的Akt触发mTORC1复合物,上调下游翻译调控因子p-S6K1和p-4EBP1,启动细胞内蛋白翻译过程,显著增强I型和III型胶原的产生和释放。
4.4 代谢重编程与能量供应
Xue等(2025)证明,Piezo1激活的Akt对大规模代谢重编程至关重要。在机械应力下,Piezo1通过钙信号通路增强葡萄糖转运蛋白Glut1和关键糖酵解酶(Aldoa、Ldha)的表达,为组织修复提供必需的碳源和能量。
此外,胶原产生依赖特定氨基酸(尤其是脯氨酸)。He等(2023)在皮肤纤维化模型中揭示了Piezo1在“精氨酸-脯氨酸代谢通路”中的关键调节功能。高刚度基质或Piezo1激动剂Yoda1处理显著增加Arg1、OAT和PYCR1等关键代谢酶的水平,促进L-精氨酸向L-脯氨酸的转化,为胶原生产提供充足原料。
五、机械失衡与病理结局
5.1 过度力学转导:纤维化瘢痕中的正反馈环路
ECM刚度驱动的受体上调:Li等(2022)发现,刚硬的ECM不仅激活Piezo1通道,还通过Integrin β1/miR-369-3p通路降低其负调节因子功能,导致Piezo1蛋白过度产生,形成危险的正反馈循环。
Piezo1-Wnt2/Wnt11-CCL24信号轴:He等(2024)在皮肤纤维化中阐明了一条独特的正反馈驱动通路。Piezo1在刚性基质上激活后,通过Wnt2(经典β-catenin通路)和Wnt11(非经典JNK通路)促使真皮成纤维细胞释放强效促纤维化细胞因子CCL24。CCL24以自分泌/旁分泌方式激活真皮成纤维细胞,组织硬化进一步升高Piezo1水平,形成自我强化循环。使用AAV敲低Piezo1可显著减少小鼠皮肤纤维化和硬度。
增生性瘢痕中的Piezo1:He等(2021)证实Piezo1在人和大鼠增生性瘢痕组织的肌成纤维细胞中表达升高。周期性机械拉伸显著增强人真皮成纤维细胞中Piezo1水平和Piezo1依赖性Ca²⁺内流,促进细胞增殖、迁移、分化和胶原合成。Piezo1抑制肽GsMTx4在体内成功保护大鼠免受拉伸触发的增生性瘢痕形成。
瘢痕疙瘩中的新机制:Liao等(2025)发现Piezo1通过促进Ca²⁺内流增强YAP核转位,激活“Piezo1-Ca²⁺-YAP”信号轴,促进促粘附和促纤维化基质成分的合成。Zhang等(2024)发现瘢痕疙瘩中存在独特的CD74⁺成纤维细胞亚群,对机械拉伸高度敏感,Piezo1-AKT信号直接促进成纤维细胞增殖和促血管生成因子分泌。
5.2 力学转导不足:慢性难愈合伤口中的Piezo1-PI3K/Akt功能障碍
与纤维化瘢痕中的过度激活相反,慢性难愈合伤口(糖尿病足溃疡、压力性溃疡、静脉性溃疡)可能反映了力学转导的缺乏或异常:
5.3 慢性伤口与纤维化瘢痕的治疗悖论
上述讨论揭示了一个根本性治疗困境:
解决策略:
时间相特异性调节:炎症期/增殖期(成纤维细胞募集和ECM沉积必需)→ 短暂Piezo1激活;重塑期(ECM交联和组织硬化增加)→ Piezo1拮抗
细胞类型特异性:Piezo1在成纤维细胞中促进迁移,在角质形成细胞中抑制迁移 → 需要细胞选择性方法(如成纤维细胞特异性AAV载体)
靶向下游效应器:mTOR(代谢重编程)、GSK3β(增殖)而非Piezo1本身,可实现更精细的治疗控制
六、与其他力学转导通路的交互
6.1 YAP/TAZ通路
Hippo-YAP/TAZ通路是经典的力学转导通路。Akt可直接磷酸化并抑制LATS1/2,促进YAP核转位。在Piezo1背景下,Ca²⁺内流可能同时激活PI3K/Akt和YAP/TAZ通路。
6.2 Rho/ROCK通路
CADM1延长的Piezo1开放可能维持FAK/RhoA/ROCK级联,形成前馈循环:Piezo1→Ca²⁺→RhoA/ROCK→膜张力增加→Piezo1再激活。ROCK还通过磷酸化PTEN和改变黏着斑分布来调节PI3K/Akt。
6.3 MAPK/ERK通路
Zhang等(2024)显示机械拉伸CD74⁺瘢痕疙瘩成纤维细胞同时激活AKT和ERK通路,提示Piezo1下游存在平行激活。
七、未来方向与临床应用前景
Piezo1在不同组织和细胞类型中呈现多样化甚至矛盾的作用,但某些机制趋势是可靠识别的。作为力学感受器,Piezo1检测组织硬度和ECM组成变化,促进Ca²⁺内流,作为上下文依赖的关键启动子,激活MAPK、TGF-β、YAP/TAZ、PI3K/Akt等通路。
现有调节剂的局限性:
未来研究方向:
优先开展整合时空监测Piezo1-PI3K/Akt活性的体内伤口模型研究
开发靶向递送系统,优化药代动力学
将Piezo1调节剂与物理模型(如高压氧、锶锌硅酸盐生物材料)联合应用,实现协同促愈合效应
八、总结
本综述系统阐明了Piezo1-Ca²⁺-PI3K/Akt信号通路在皮肤伤口愈合中的分子机制与功能意义:
| | |
|---|
| | |
| Integrin-FAK协同通路 | 验证最充分 | |
| | |
| | |
| 增殖(Akt-GSK3β-Cyclin D1) | 部分验证 | |
| 迁移(Piezo1-FAK-PI3K/Akt) | 步骤验证,未连接 | |
| 代谢重编程(Akt-mTOR) | 部分验证 | |
| 肌成纤维细胞分化(与TGF-β/Smad协同) | 部分验证 | |
核心结论:Piezo1-Ca²⁺-PI3K/Akt信号轴是皮肤成纤维细胞中上下文依赖的力学转导汇聚节点,通过多条并行分子桥梁将物理机械力转化为细胞内生化信号,精细调控成纤维细胞的增殖、迁移、代谢重编程和肌成纤维细胞分化。该轴的失调是慢性伤口(信号不足)和病理性瘢痕(信号过度)的共同机制基础,为开发基于力学调控的创新伤口治疗策略提供了坚实的理论框架和治疗靶点。
*参考文献:Wang S, Li Y, Han Y, et al. The Piezo1-Ca²⁺-PI3K/Akt Signaling Axis As a Context-Dependent Mechanotransduction Node During Skin Wound Healing. iScience, 2026.*

