近日,海南医科大学生命科学与医学技术学院、国家卫生健康委员会热带病防治重点实验室,在Elsevier旗下中国科学院一区《Chemical Engineering Journal》期刊发表题为“A stimuli-responsive polymeric ferroptosis drug delivery system for treatment of liver metastases”的研究性论文。该研究聚焦肿瘤肝转移这一临床治疗难题,构建了一种肿瘤微环境响应型聚合物纳米递药系统,为肝转移精准干预提供了新的研究思路和实验依据。
肝转移是多种恶性肿瘤患者死亡的重要原因之一,具有微环境复杂、治疗耐受强、预后差等特点。针对现有治疗手段在肿瘤穿透性、靶向性和安全性等方面存在的不足,研究团队从肝转移微环境特征入手,系统分析了铁死亡相关分子和基质金属蛋白酶在肝转移中的作用。研究发现,SLC7A11和MMP-9在肝转移组织中高表达,并与患者不良预后密切相关,提示二者可能是干预肝转移进展的重要靶点。
基于上述发现,团队设计构建了肿瘤微环境响应型纳米药物NP-R-M。该系统将小分子铁死亡诱导剂RSL3与可被MMP-9特异性切割激活的蜂毒肽衍生功能分子协同组装于纳米载体中。进入肿瘤部位后,纳米系统可借助MMP-9高表达环境实现响应性释放,其中蜂毒肽增强肿瘤细胞膜通透性,促进RSL3高效进入肿瘤细胞,进而诱导活性氧积累、脂质过氧化和线粒体功能损伤,最终触发肿瘤细胞铁死亡。研究还表明,该纳米系统在入血后形成的蛋白冠有助于提高其对肝转移灶的富集能力,同时降低全身毒性。
在小鼠肝转移模型中,NP-R-M表现出良好的体内治疗效果。实验结果显示,该系统可显著增强肿瘤部位聚集,明显降低肝转移负荷并延长荷瘤小鼠生存时间。进一步机制研究发现,NP-R-M不仅能够直接诱导肿瘤细胞死亡,还可有效重塑肝转移免疫微环境,促进CD8+ T细胞及Granzyme B+ CD8+ T细胞浸润,同时减少M2型巨噬细胞浸润,从而形成“直接杀伤+免疫调控”协同抗肿瘤作用。
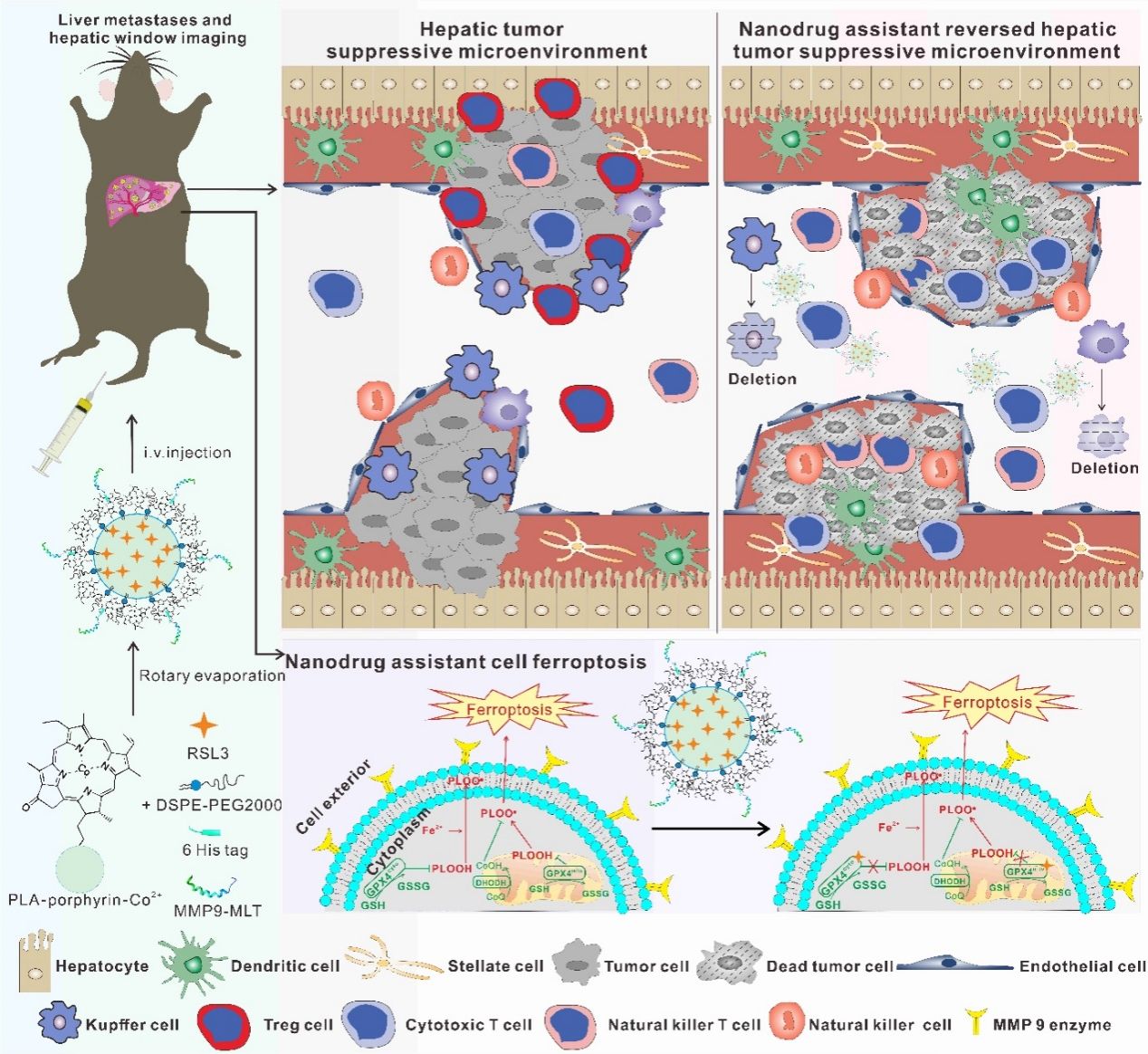
该研究将酶响应释放、膜通透增强、铁死亡诱导与免疫微环境重塑有机结合,拓展了铁死亡策略在转移性肿瘤治疗中的应用边界,也为肝转移及其他难治性实体瘤的纳米药物设计提供了新的理论基础和技术路径。我校青年教师邓得强为本论文的第一作者,金红林教授为通讯作者。该成果以海南医科大学为第一完成单位,研究得到国家自然科学基金、湖北省自然科学基金青年项目等课题资助。
通讯员:邓得强
一审:王俊杰
二审:金红林
三审:李春报