
北京时间4月16日,国际学术期刊《自然·纳米技术》(Nature Nanotechnology)在线发表了金红林教授团队联合中国科学院长春应用化学研究所和美国纽约州立大学布法罗分校合作完成的题为“Enhancing Antitumor Nanovaccine Efficacy via Integrated Cholesterol Modulation In Situ”的研究成果。
该研究聚焦肿瘤疫苗“激活不强”的核心难题,创新性地从细胞膜胆固醇这一关键因素入手,提出通过降低树突状细胞膜胆固醇来增强抗原递呈能力。研究团队构建了兼具抗原递送与胆固醇调控功能的纳米疫苗体系,并首次证实膜胆固醇耗竭能够显著提升免疫激活效率。研究发现,这一过程如同为免疫细胞之间的相互作用“打开加速通道”,不仅增强了树突状细胞与T细胞的接触与免疫突触形成,还通过重塑膜胆固醇微结构并阻断胞葬通路,显著提升CD8⁺T细胞的增殖与抗肿瘤功能,最终在多种肿瘤模型中实现显著抑瘤效果。该成果为开发新一代高效肿瘤纳米疫苗提供了重要方向。
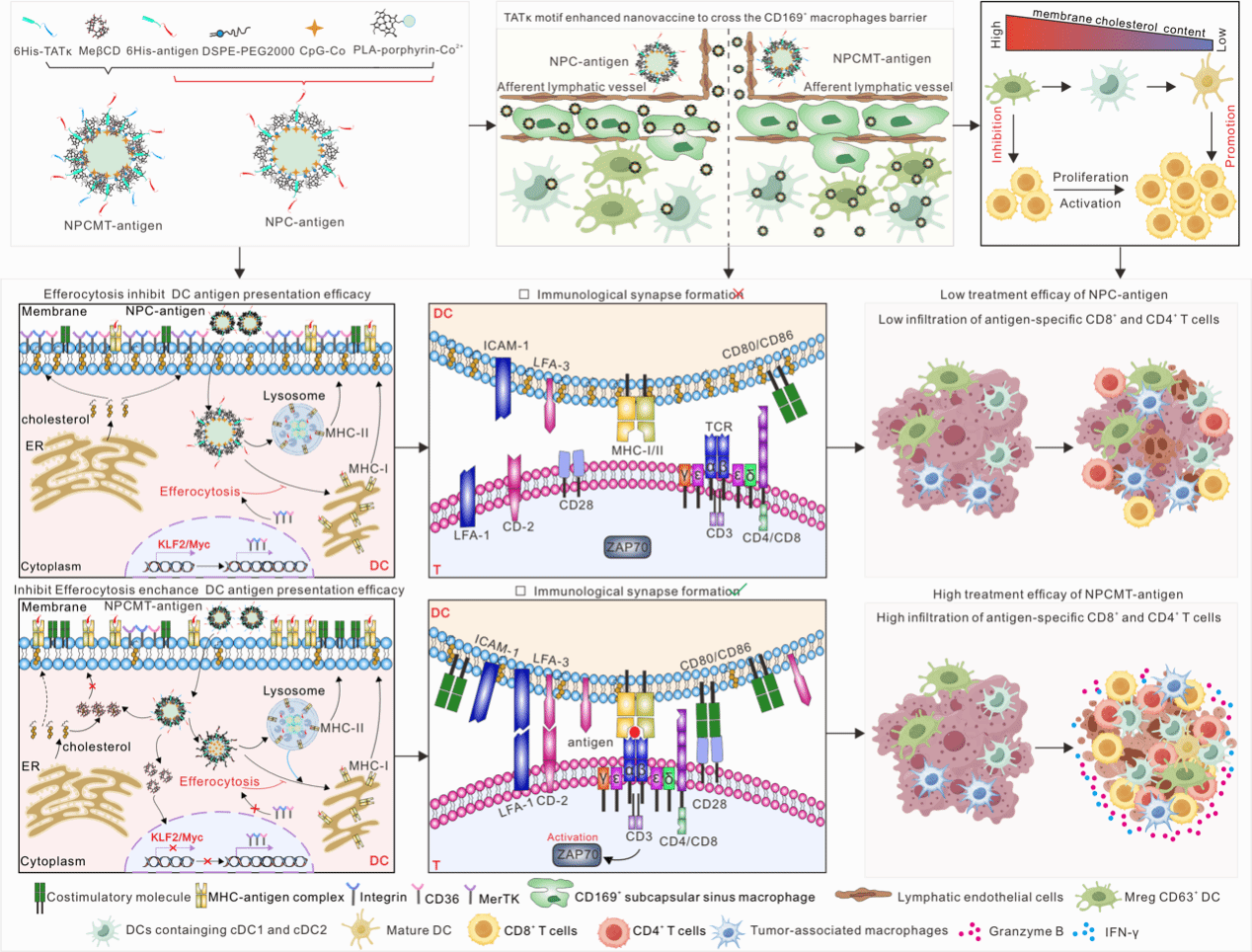
用于胆固醇调控与细胞穿透协同增强纳米疫苗抗肿瘤免疫的示意模型
揭示限制纳米疫苗疗效的关键机制
该研究聚焦肿瘤疫苗中抗原递呈效率不足这一核心瓶颈问题,创新性发现树突状细胞膜胆固醇水平在调控抗原交叉递呈过程中发挥关键作用。研究表明,抗原递呈效率受限并非仅由抗原递送不足所致,更与细胞膜微环境中胆固醇分布密切相关,从而揭示了一种此前未被充分认识的免疫调控机制。
构建协同调控的新型纳米疫苗体系
基于这一发现,研究团队设计并构建了一种兼具“抗原递送+胆固醇调控”功能的纳米疫苗体系,实现了对树突状细胞膜胆固醇的原位调控。该体系在递送抗原的同时,能够有效降低细胞膜胆固醇水平,从而协同增强抗原加工与递呈能力。
如果将抗原递呈过程比作免疫系统识别肿瘤的“信息传递通路”,那么胆固醇则如同调控通路效率的“关键阻力因素”。该研究通过精准调控这一因素,相当于为免疫系统“疏通通路”,显著提升信息传递效率。
重塑抗原递呈与免疫激活过程
研究发现,膜胆固醇的降低能够显著增强树突状细胞与T细胞之间的相互作用频率,并促进免疫突触的形成。这一过程如同加强免疫细胞之间的“信号连接节点”,从而有效放大免疫激活信号。
在机制层面,该纳米疫苗通过重塑膜胆固醇微结构并阻断胞葬通路(efferocytosis),显著提升抗原交叉递呈效率,进一步增强CD8⁺ T细胞的激活与增殖能力,从而在多个肿瘤模型中实现显著的抗肿瘤效果。
为肿瘤免疫治疗提供新路径
在转化应用层面,该研究具有重要意义。研究团队在多种肿瘤模型中(包括B16黑色素瘤、4T1乳腺癌及肺转移瘤模型)系统评估了该纳米疫苗的抗肿瘤效果,均显示出显著的抑瘤作用。其中,在人源化小鼠模型中进一步验证了其在接近人体免疫环境下的有效性,证实该体系能够有效促进CD8⁺ T细胞的激活与扩增,并显著增强抗肿瘤免疫反应。
综上,该研究表明,通过靶向调控树突状细胞膜胆固醇水平,不仅可以系统性提升抗原递呈效率,还能够重塑免疫细胞间的相互作用模式,从而实现对抗肿瘤免疫反应的精准放大。该研究为开发新一代高效肿瘤纳米疫苗及免疫治疗策略提供了重要依据。
本研究由金红林教授团队牵头完成,课题组邓紫晗博士生、卢利森副研究员和徐天兵博士生为本文的共同第一作者。华中农业大学生物医学与健康学院孙耀教授、中国科学院长春应用化学研究所丁建勋教授与美国纽约州立大学布法罗分校Jonathan F. Lovell教授为本文的共同通讯作者。研究工作还得到了武汉大学人民医院等单位研究人员的重要支持与贡献。
原文链接:https://www.nature.com/articles/s41565-026-02153-w
通讯员:卢利森
一审:王俊杰
二审:金红林
三审:李春报